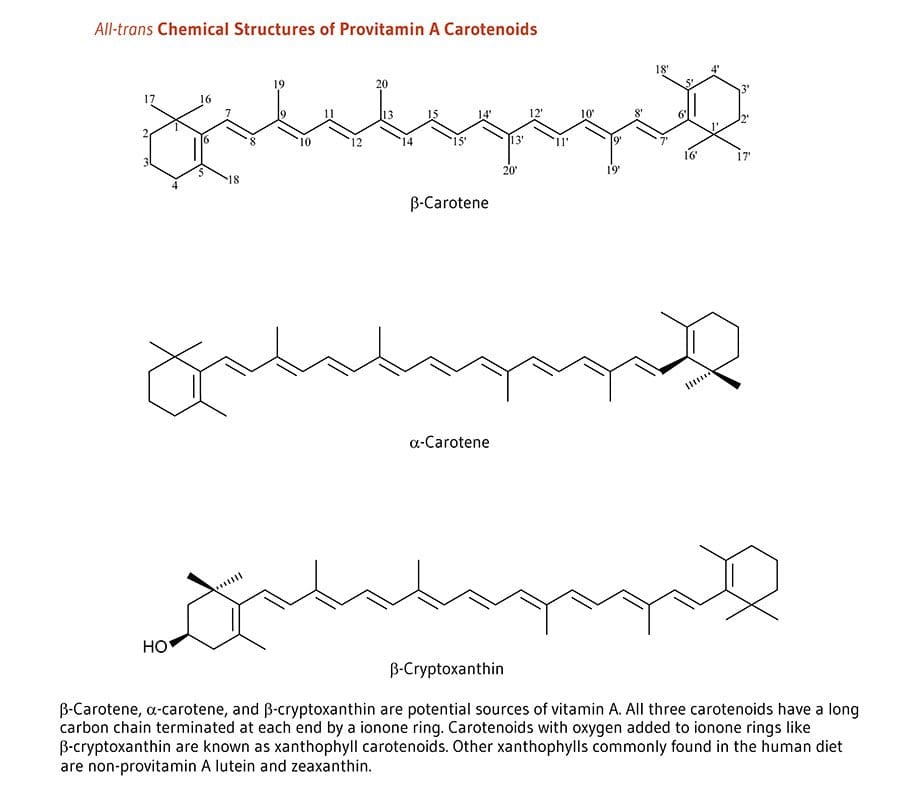
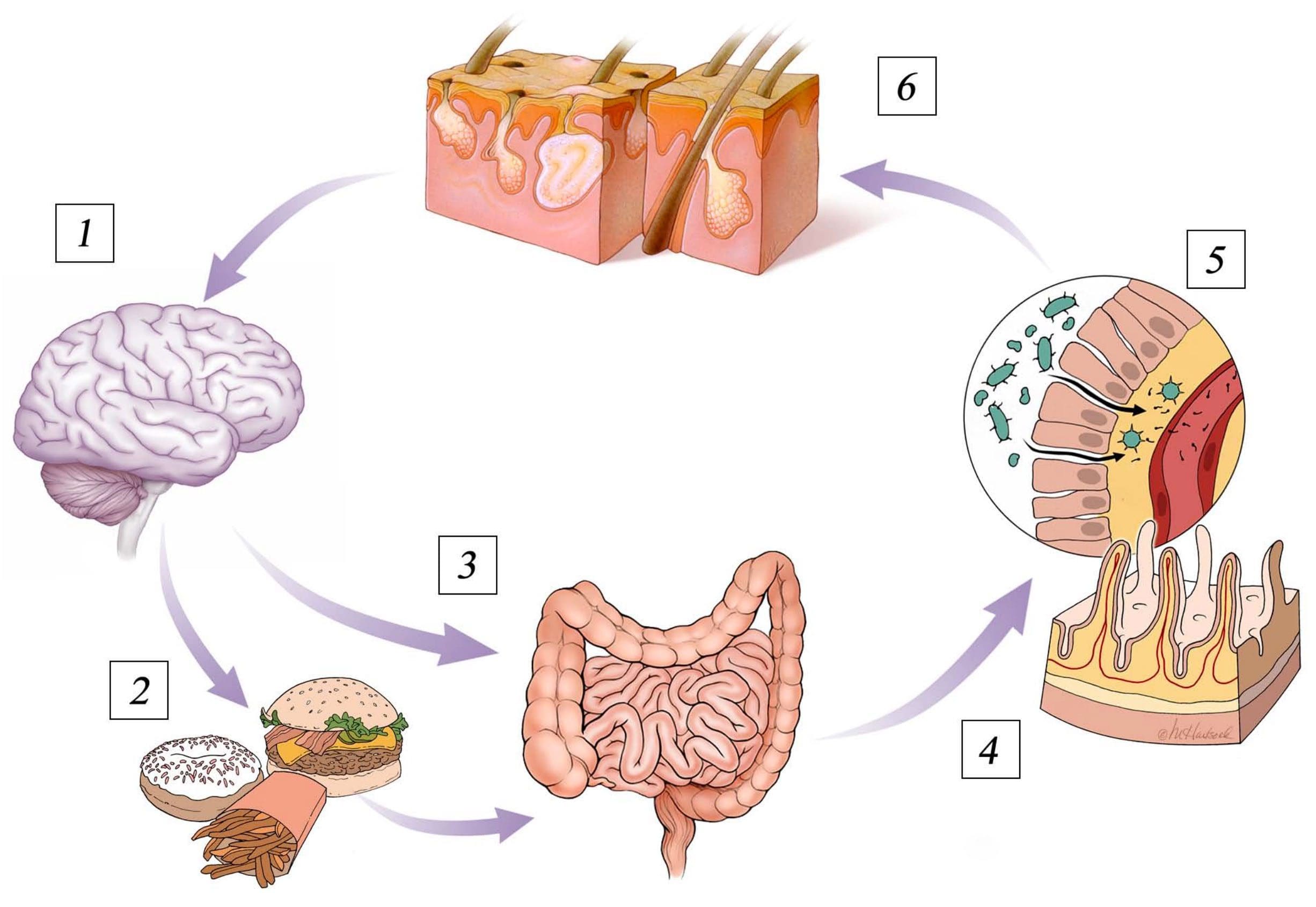
פסוריאזיס תקציר
פסוריאזיס היא הפרעה חיסונית שכיחה בתאי T, המאופיינת על ידי לוחיות מוגבלות, אדומות ומעבות, עם סולם כסף לבן מעל. זה קורה ברחבי העולם, אם כי השכיחות נמוכה יותר באקלים חם, חם יותר. הסיבה העיקרית לפסוריאזיס אינה ידועה. במהלך מחלה פעילה המדינה, מנגנון דלקתי הבסיסית היא לעתים קרובות מעורבים. טיפולים קונבנציונליים רבים מתמקדים בדיכוי סימפטומים הקשורים בפסוריאזיס ויש להם תופעות לוואי משמעותיות. מאמר זה סוקר כמה מן הגישות הטבעיות שנחקרו לטיפול בפסוריאזיס, תוך התייחסות לגורם הבסיסי שלו. (אלטרנטיבי מד 2007; 12 (4): 319-330)
מבוא
ההתקדמות הגנטית והאימונולוגית האחרונה הגדילה מאוד את ההבנה של הפתוגנזה של פסוריאזיס כהפרעה דלקתית כרונית מתווכת חיסונית. נראה שהפגם החיסוני העיקרי בפסוריאזיס הוא עלייה באיתות תאים באמצעות כימוקינים וציטוקינים הפועלים על ביטוי גנים מווסת וגורמים לשגשוג יתר של קרטינוציטים. הבנה חדשה של מחלה מורכבת זו זירזה את הפיתוח של טיפולים ביולוגיים ממוקדים. עם זאת, טיפולים מהפכניים אלו אינם נטולי סיכון פוטנציאלי. סקירה של טיפולים טבעיים אלטרנטיביים מספקת כמה אפשרויות להגברת הבטיחות והיעילות בטיפול בפסוריאזיס. פסוריאזיס � פתופיזיולוגיה, גישות קונבנציונליות ואלטרנטיביות לטיפול מייקל טראוב, ND, ו-Keri Marshall MS, ND
אֶפִּידֶמִיוֹלוֹגִיָה
השכיחות של פסוריאזיס משתנה במידה רבה בהתאם לאתניות. פסוריאזיס מתרחשת בדרך כלל בקווקזים, עם התרחשות משוער של מקרים 60 לכל 100,000 / שנה באוכלוסייה זו. השכיחות שלה בארצות הברית היא 2-4 אחוז, למרות שזה נדיר או נעדר ב Native American ואוכלוסיות אפריקאיות מסוימות. אמנם נפוץ ביפן, זה הרבה פחות נפוץ בסין, עם אומדן משוער של 0.3 אחוזים. השכיחות באוכלוסייה הכללית של צפון אירופה וסקנדינביה היא 1.5-3 אחוזים. נשים וגברים מושפעים במידה שווה ממצב זה. התצפית כי קו הרוחב משפיע על שכיחות היא ככל הנראה קשור ההשפעה החיובית של אור השמש על המחלה. 1 למרות פסוריאזיס יכול להתרחש בכל גיל, הגיל הממוצע של הופעת פסוריאזיס פלאק כרונית נאמד ב 33 שנים, עם 75 אחוז של המקרים יזמה לפני גיל 46.2 גיל הופעת נראה מעט מוקדם יותר בנשים מאשר גברים. מחקרים אורךיים מצביעים על רמיסיה ספונטנית עלולה להתרחש בכשליש מהחולים עם פסוריאזיס. 3
פתופיזיולוגיה
עד לאחרונה פסוריאזיס נחשבה להפרעה של קרטינוציטים אפידרמיס; עם זאת, כיום היא מוכרת בעיקר כהפרעה בתיווך חיסוני. על מנת להבין נכון את חוסר התפקוד החיסוני הקיים בפסוריאזיס, הכרחי להבין את התגובה החיסונית הרגילה של העור. העור הוא איבר לימפואידי ראשוני עם מערכת מעקב אימונולוגית יעילה המצוידת בתאים מציגי אנטיגן, קרטינוציטים מסנתזים ציטוקינים, תאי T אפידרמוטרופיים, תאי אנדותל נימים עוריים, צמתים מנקזים, תאי מאסט, מקרופאגים של רקמות, גרנולוציטים, תאים פיברובלסטים ותאי לא לנגרנים. לעור יש גם בלוטות לימפה ולימפוציטים T במחזור. יחד תאים אלו מתקשרים באמצעות הפרשת ציטוקינים ומגיבים בהתאם באמצעות גירוי על ידי חיידקים, כימיקלים, אור אולטרה סגול (UV) וגורמים מגרים אחרים. הציטוקין העיקרי המשתחרר בתגובה להצגת אנטיגן הוא tumor necrosis factor-alpha (TNF-?). ככלל, זהו תהליך מבוקר אלא אם העלבון לעור ממושך, ובמקרה זה ייצור ציטוקינים לא מאוזן מוביל למצב פתולוגי כמו פסוריאזיס.
נמשך הוויכוח אם פסוריאזיס היא הפרעה אוטואימונית או הפרעה בתפקוד החיסוני של T-helper 1 (Th1). הפעלת תאי T, TNF-?, ותאי דנדריטים הם גורמים פתוגניים המגורים בתגובה לגורם מעורר, כגון פציעה פיזית, דלקת, חיידקים, וירוסים או גמילה מתרופות קורטיקוסטרואידים. בתחילה, תאים דנדריטים לא בשלים באפידרמיס מגרים תאי T מבלוטות לימפה בתגובה לגירוי אנטיגן שטרם זוהה. החדירת הלימפוציטית בפסוריאזיס היא בעיקר תאי CD4 ו-CD8 T. מולקולות הידבקות המעודדות היצמדות לויקוציטים מתבטאות מאוד בנגעים פסוריאטיים.4 לאחר שתאי T מקבלים גירוי והפעלה ראשונית, מתרחשת סינתזה של mRNA עבור אינטרלוקין-2 (IL-2), וכתוצאה מכך עולה שלאחר מכן בקולטני IL-2. פסוריאזיס נחשבת למחלה דומיננטית של Th1 עקב העלייה בציטוקינים של מסלול Th1 � אינטרפרון גמא (IFN-?), IL-2 ואינטרלוקין 12 (IL-12) � הנמצאים בפלאקים פסוריאטיים.
הגידול ב-IL-2 מתאי T משופעלים ו-IL-12 מתאי לנגרהנס מווסתים בסופו של דבר גנים המקודדים לשעתוק של ציטוקינים כגון IFN-?, TNF-? ו-IL-2, האחראים על התמיינות, הבשלה ושגשוג של תאי T לתוך תאי אפקטור זיכרון. בסופו של דבר, תאי T נודדים לעור, שם הם מצטברים סביב כלי דם עוריים. אלו הם הראשונים בסדרה של שינויים אימונולוגיים שגורמים להיווצרות נגעים פסוריאטיים חריפים. מכיוון שהתגובה החיסונית המתוארת לעיל היא תגובה נורמלית במקצת לגירוי אנטיגן, עדיין לא ברור מדוע הפעלת תאי ה-T המתרחשת, ואחריה נדידה של לויקוציטים לאחר מכן לאפידרמיס ולדרמיס, יוצרת שגשוג מואץ של תאי. ויסות גנים משופר עשוי להיות גורם סיבתי. גורם גדילה אנדותל וסקולרי (VEGF) ואינטרלוקין-8 המשתחררים מקרטינוציטים עשויים לתרום לאוסקולריזציה הנראית בפסוריאזיס.5
נראה כי תאים דנדריטים מעורבים בפתוגנזה של פסוריאזיס. סוג אחד של תאים דנדריטים המעורבים הוא תאי לנגרהנס, הזקיף החיצוני ביותר של מערכת החיסון שמזהה ולוכד אנטיגנים, נודד לבלוטות לימפה מקומיות ומציג אותם לתאי T. ההפעלה של לימפוציטים T משחררת ציטוקינים פרו-דלקתיים כגון TNF-? שמובילים לשגשוג קרטינוציטים. תגובה היפר-פרוליפרטיבית זו מקטינה את זמן המעבר האפידרמיס (הזמן המשוער שלוקח להבשלה נורמלית של תאי עור) מ-28 ימים ל-2-4 ימים ומייצרת את הפלאק הקשקשי האדמתי האופייני לפסוריאזיס. הבנה זו של מנגנונים פתוגניים הובילה לפיתוח ושימוש טיפולי ב-TNF-? סוכני חסימה.
לכ-30 אחוז מהאנשים עם פסוריאזיס יש היסטוריה משפחתית של המחלה אצל קרוב משפחה מדרגה ראשונה או שנייה. לפחות תשעה לוקוסים של רגישות כרומוזומלית הובהרו (PSORS1-9). HLA-Cw6 הוא גורם מכריע של ביטוי פנוטיפי. נמצא קשר עם ה-PSORS עם פולימורפיזמים תפקודיים בגנים משנים המתווכים דלקת (למשל, TNF-?) וצמיחת כלי דם (למשל, VEGF).6
ידוע שפסוריאזיס מתפתחת אצל מושתלי מח עצם מתורמים עם פסוריאזיס, מתנקה אצל מקבלי תורמים ללא פסוריאזיס, ושתרופות מדכאות חיסון יעילות בהפחתת פסוריאזיס.7,8 בהתחשב בנטייה הגנטית למחלה זו, מה ניתן לעשות כדי להפחית את הביטוי הגנטי מלבד פנייה לטיפולים מדכאים חיסוניים? גישה נטורופתית מורכבת משינוי תזונתי,�צום טיפולי, תוספי אומגה 3, תרופות טבעיות אקטואליות, צמחי מרפא וניהול מתח.
Pizzorno ומורי מציעים שהאנטיגנים הלא מזוהים הנ"ל נובעים מעיכול חלבון לא שלם, חדירות מוגברת של המעי ואלרגיות למזון; מעי toxemia (endotoxins); ליקוי בכבד דטוקסיפיקציה; חסר חומצה מרה; צריכת אלכוהול; צריכה מוגזמת של שומנים מן החי; חסרים תזונתיים (ויטמינים A ו- E, אבץ וסלניום); ו stress.XNXX השערות אלה, אם כי סביר, לא נבדקו כראוי.
תחלואה משותפת
פסוריאזיס קשורה למספר מחלות נלוות, כולל ירידה באיכות החיים, דיכאון, סיכון קרדיווסקולרי מוגבר, סוכרת מסוג 2, תסמונת מטבולית, סרטן, מחלת קרוהן ודלקת מפרקים פסוריאטית. עדיין לא ברור אם סוגי הסרטן, בפרט סרטן העור ולימפומה, קשורים לפסוריאזיס או לטיפול בה. פוטותרפיה וטיפול מדכא חיסון יכולים להגביר את הסיכון לסרטן עור שאינו מלנומה, למשל.10
דאגה מיוחדת היא הקשר שנצפה בין פסוריאזיס למחלות לב וכלי דם. עדות לכך היא שהפסוריאזיס הוא גורם סיכון עצמאי למחלות לב וכלי דם. 11 דיסליפידמיה, הסתיידות הכלילית, גדילה גבוהה של C-reactive protein (CRP), ירידה בחומצה פולית ו hyperhomocysteinemia נמצאות עם תדירות גבוהה משמעותית בחולי פסוריאזיס. 12 דלקות היא נושא משותף שני התנאים הבסיסיים, המאופיינים על ידי נוכחות של ציטוקינים פרו דלקתיים הפעלה אנדותל.
התהליכים הדלקתיים העומדים בבסיס הפסוריאזיס מרמזים גם על אפשרות של מחסור בחומצת שומן אומגה 3, חומצת שומן פולית וויטמין B12, שנמצאים לעתים קרובות גם במחלות לב וכלי דם.13 גבוה הומוציסטאין ורמות חומצה פולית מופחתות מתואמים עם פסוריאזיס אזור וחומרה אינדקס (PASI). קצב תחלופה מהיר של תאי עור בפסוריאזיס עלול לגרום לניצול מוגבר של חומצה פולית ולמחסור שלאחר מכן.14 מחברו של מחקר אחד מסיק: "תוספת תזונתית של חומצה פולית, B6 ו-B12 נראית סבירה בחולי פסוריאזיס, במיוחד אלו עם הומוציסטאין גבוה, נמוך חומצה פולית וגורמי סיכון קרדיווסקולריים נוספים.�15
דלקת מפרקים פסוריאטית היא מצב קליני המתרחש ב- 25 אחוז של אנשים שסבלו מפסוריאזיס. 16 בכ- 10 בקירוב מאוכלוסיה זו, הסימפטומים הארתריטיים מקדימים את נגעי העור. דלקת מפרקים פסוריאטית מופיעה לעיתים קרובות כדלקת מפרקים דלקתית סרונגגטיבית, עם מצגת קלאסית המורכבת מאוליגוארתריטיס, מעורבות במפרקים בין-מפלתיים דיסטליות, דקטיליטיס (דלקת הספרות) ודלקות קלקניאליות.
התנגשות הדעות אם מצב העור ודלקת מפרקים מייצגים ביטוי שונה של אותה מחלה. עדויות גנטיות, מחקרים אימונולוגים ושינויי תגובה לטיפול, מצביעים על כך שהם עשויים להיות שני מצבים שונים, אולי עם דלקת בסיסית דומה ואי סדירות של המערכת החיסונית. 17,18
למרות pustulosis palmoplantar (PP) מתואר לעתים קרובות כסוג של פסוריאזיס, דמוגרפיה שונים ניתוח גנטי מציע אטיולוגיה שונה מאשר פסוריאזיס. על המראה, PP יש pustules סטרילי צהבהב המופיעים על כפות הידיים ואת הסוליות. רק 25 אחוז מהנשאלים מדווחים על פסוריאזיס שלפוחית כרונית. PP מתרחשת בתדירות גבוהה יותר אצל נשים (9: 1 / נקבה: זכר) ו- 95 אחוז מהאנשים שנפגעו יש היסטוריה עכשווית או קודמת של עישון. כתוצאה מכך, PP עשוי להיחשב מצב חולני משותף ולא צורה נפרדת של פסוריאזיס. 19
קריטריונים לאבחון
פסוריאזיס מסווג למספר תת-סוגים, עם הפלאק הכרוני (פסוריאזיס וולגאריס), המהווה כ -9% מהמקרים. חדות באופן קיצוני plesques scurating אריאליטיס כסוף להתרחש הנפוץ ביותר על פני extensor של המרפקים, הברכיים, הקרקפת, המקודש, אזורים המפשעה. אזורים מעורבים אחרים כוללים את האוזניים, פין העטרה, אזור הפריאנל, ואתרים של טראומה חוזרת. מקרה דלקתי פעיל של פסוריאזיס יכול להדגים את תופעת Koebner שבה נגעים חדשים נוצרים במקום של טראומה או לחץ.
בעתיד, פסוריאזיס שלפוחית כרונית עשויה להימצא מורכבת מכמה תנאים קשורים עם מאפיינים פנוטיפיים וגנוטיפיים מובהקים, המספקים הסבר לתגובתו המשתנה לטיפול, במיוחד עם גורמים ביולוגיים.
פסוריאזיס הפוכה מתרחשת באתרים משולבים ובקפלי עור והיא אדומה, מבריקה ולרוב ללא קשקשים. סבופסוריאזיס, שלעתים קרובות מבולבלת עם סבוריאה דרמטיטיס, מאופיינת בקשקשים שומניים�בגבות, בקפלים nasolabial, ובאזורים postauricular ו היוקרתי.
פסוריאזיס גוטית חריפה מתרחשת אצל ילדים, מתבגרים ומבוגרים צעירים כשבועיים לאחר זיהום סטרפטוקוקאלי ביתא חריף, כגון דלקת שקדים או דלקת הלוע, או זיהום ויראלי. זה מתבטא כמו התפרצות אריתמטית, papular עם נגעים פחות 1 ס"מ בקוטר על תא המטען והגפיים. פסוריאזיס מחוספס חריף הוא בדרך כלל מוגבל עצמית, פתרון בתוך 3-4 חודשים. מחקר אחד הראה כי רק שליש מהחולים עם פסוריאזיס מקוטע מפתחים פסוריאזיס קלאסי של הפלאק. 20
Porular פסוריאזיס (פון Zumbusch) היא גם התפרצות psoriatic חריפה. החולה מציג עם חום ופסטולות קטנות, מונומורפיות, כואבות, סטריליות, לעיתים קרובות מזרזות על ידי זיהום בינכאני או נסיגה פתאומית של סטרואידים מקומיים או מערכתיים סופר-פוטנטיים. זה יכול להיות מקומי לכפות הידיים ואת כפות (palmar-plantar פסוריאזיס) או שזה יכול להיות generalised ו פוטנציאלי החיים.
פסוריאזיס אריתרודרמי, גם מסכן חיים, כולל את כל שטח הגוף ויכול לגרום היפותרמיה, hypoalbuminemia, אנמיה, זיהום, ואת כישלון הלב גבוה פלט.
מחלת הציפורניים פסוריאטית מתרחשת בכ- 50 אחוזים מחולי הפסוריאזיס, ובדרך כלל מתבטאת בהדבקה. שינויים מסמר אחרים יכולים לכלול onycholysis, שינוי צבע, עיבוי, ניוון.
גורמי סיכון
פיתוח של פסוריאזיס כרוך באינטראקציה של מספר גורמי סיכון גנטיים עם גורמים סביבתיים, כגון זיהום סטרפטוקוקלי בטא-המוליטיס, HIV, מתח ותרופות (למשל, חוסמי בטא וליתיום). כפי שצוין לעיל, חומצה פולית וויטמין BXNXX יכול גם predispose. בנוסף, ישנן עדויות כי אלכוהוליזם, עישון סיגריות, השמנה, סוג 12 סוכרת, תסמונת מטבולית להגדיל את הסיכון לפתח פסוריאזיס.
למעט VEGF, לא נמצא סמנים ביולוגיים כמנבאים אמין של פעילות פסוריאזיס. CRP, מולקולות הדבקה מסיסות, וקולטני ציטוקינים מסיסים נחקרו אך אינם תואמים את חומרתם. 21
טיפול קונבנציונאלי
טיפול קונבנציונלי של פסוריאזיס מבוסס על מידת החומרה. טיפול פסוריאזיס קל ומוגבל כולל קורטיקוסטרואידים מקומיים, טארס, אנתרלין, calcipotriene (אנלוגיית ויטמין D3), tazarotene (רטינואיד) ו phototherapy. רופאים יכולים להגדיר ציפיות ריאליות לטיפול, לתת למטופל שליטה על המחלה ללא ציפייה לריפוי מלא. הקרקפת פסוריאזיס מגיבה בדרך כלל שמפו חומצה סליצילית.
נגיף UVB צר יותר יעיל אך בטוח יותר מ PSoralen בתוספת UV אולטרה סגול (PUVA), אשר נושא עמו סיכון מוגבר לסרטן העור. חשיפה לשמש היא צורה אחרת של פוטותרפיה. חשיפה UV מפחיתה הצגה אנטיגן משפיע על איתות תא, לטובת פיתוח של T-Helper 2 (Th2) תגובות החיסונית. אנטיגן מציג תאים Langerhans הם ירדו במספר והן function.22
שילוב מקומי של calcipotriene ו-betamethasone (Taclonex�) הראה יעילות רבה יותר בפסוריאזיס חמורה מאשר טיפול יחיד עם אחד מהם לבד.23
יש לשקול את עמידת החולה בעת פיתוח תוכנית טיפול. השימוש בתמיסות אקטואליות פחות ותכשירי קצף של קורטיקוסטרואידים מקומיים ו calcipotriene (בהשוואה למשחות ולמשחות) יכול לשפר את התאימות.
טיפול סיסטמי בפסוריאזיס חמור כולל בדרך כלל שימוש ברטינואידים אוראליים, מטוטרקסטים, ציקלוספורין וסוכנים ביולוגיים שיכולים להשפיע באופן משמעותי על מערכות גוף אחרות.
הרטינואיד אוראלי אציטרטין הוא טרטוגני והוא הופך לאטרטינט עם בליעת אלכוהול במקביל. לאטרטינט יש זמן מחצית חיים ארוך יותר והוא טרטוגני יותר מאציטרטין. מטופלות חייבות להשתמש בשתי צורות של אמצעי מניעה ואסור להכנס להריון לפחות שלוש שנים לאחר הטיפול. בגלל אינטראקציה אפשרית עם אמצעי מניעה דרך הפה, יש להימנע משורש ג'ון (Hypericum perfoliatum). תופעות לוואי אחרות כוללות השפעות רירית עוריות, טריגליצרידים גבוהים, התקרחות וצהבת. טיפול באציטרטין דורש ניטור תכוף של ספירת דם, פרופילים מטבוליים מקיפים ובדיקת שתן. אסטרטגיות להפחתת רעילות אציטרטין כוללות שימוש לסירוגין, הפחתת מינון התחזוקה לכל יום אחר או כל יום שלישי, טיפול משולב עם PUVA או קלציפוטריאן מקומי, דיאטה דלת שומן, פעילות גופנית אירובית, תוספת שמן דגים, וכאמור לעיל, הימנעות מאלכוהול.
Methotrexate (MTX) הוא הגורם המערכתי הנפוץ ביותר לפסוריאזיס, ומכיוון שהוא זמין כבר 35 שנים, רוב רופאי העור מרגישים בנוח עם השימוש בו. Methotrexate מעכב dihydrofolate reductase (כתוצאה מכך למחסור בחומצה פולית פעילה) ומעורר אדנוזין A1, אגוניסט אנטי דלקתי חזק. מנגנון הפעולה שלו עשוי להיות מורכב עוד יותר, עדות לכך שקפאין מעכב את ההשפעות האנטי דלקתיות של MTX בדלקת מפרקים שגרונית אך לא בפסוריאזיס או דלקת מפרקים פסוריאטית.24 ההשפעות השליליות החמורות הנפוצות ביותר של MTX הן דיכוי מיאלוס ופיברוזיס בכבד. בעוד דיכוי מיאלו אינו מתרחש לעתים קרובות, מטופלים המשתמשים ב-MTX מדווחים לעתים קרובות על תסמינים של כאבי ראש, עייפות ובחילות. תוספת פולאט מפחיתה את השכיחות של אנמיה מגלובלסטית, רעילות בכבד ואי סבילות במערכת העיכול. למרות שנראה כי חומצה פולית וחומצה פולית יעילה באותה מידה, חומצה פולית היא חסכונית יותר.25 עם זאת, מחקר כפול סמיות שנערך לאחרונה על 22 חולי פסוריאזיס היציבים בטיפול ארוך טווח ב-MTX גילה כי חומצה פולית הפחיתה את היעילות של MTX בשליטה בפסוריאזיס . החולים חולקו באופן אקראי לקבלת חומצה פולית במינון של 5 מ"ג ליום או פלצבו למשך 12 שבועות. ה-PASI הממוצע עלה (הוחמר) בקבוצת החומצה הפולית, מ-6.4 בקו הבסיס ל-10.8 לאחר 12 שבועות. בקבוצת הפלצבו, ה-PASI הממוצע ירד מ-9.8 בנקודת ההתחלה ל-9.2 ב-12 שבועות (p<0.05 עבור ההבדל בשינוי בין הקבוצות).26
Cyclosporine, תרופה חזקה ורעילה, נחשבת במקרים מסוימים במקרים שאינם בשליטת acitretin, PUVA או MTX, אך היא מתווית בחולים עם תפקוד כלייתי חריג, יתר לחץ דם לא תקין, תפקוד לקוי או אימונוס דיכוי. שימוש ממושך גורם בהכרח לנזק כלייתי. לחץ דם וניטור קריאטינין הוא חיוני.
סוכנים ביולוגיים חוסמים הפעלת תאי T ו-TNF-?. Alefacept (Amevive�) מפריע להפעלת תאי T ומפחית את מחזור תאי CD 45 RO+ T. תרופה זו היא חלבון היתוך של קולטן Fc של IgG1 ו-LFA3 אנושיים, ליגנד מעורר שיתוף, המקיים אינטראקציה עם CD2 על פני השטח של תאי T. יש לנטר תאי CD4 מדי שבוע במהלך הטיפול בחומר זה.
Efalizumab (Raptiva�) הוא נוגדן הומני ל-CD11 המפריע לסחר בתאי T לרקמות דלקתיות ומונע הפעלה של תאי T. למרות שהוא יעיל במהירות, ריבאונד עשוי להתרחש.
TNF-? חוסמים מווסתים את ביטוי הגנים הפרו-דלקתיים והופכים את הפנוטיפ הפסוריאטי. Etanercept (Enbrel�) הוא חלבון היתוך המכוון נגד TNF-?. Infliximab (Remicade�) הוא נוגדן חד שבטי כימרי עכבר/אנושי נגד TNF-? מסיס וקשור לתאים, בעוד ש-adalimumab (Humira�) הוא נוגדן חד שבטי אנושי נגד TNF-?. אלה TNF-? מעכבים ניתנים בהזרקה ונקשרו בהשראת תופעות אוטואימוניות שונות. כמו TNF-? עצמו, TNF-? למעכבים יכולות להיות פעילות פרו-דלקתית וגם אנטי-דלקתית. רק בגלל שחומר מסוים חוסם TNF-?, זה לא בהכרח מועיל לפסוריאזיס. אם מטופל בעל נטייה גנטית לייצור יתר של TNF-?, ייתכן שחסימתו לא תספיק כדי לייצר תועלת.27 סיכונים אפשריים של TNF-? חוסמים כוללים הפעלה מחדש של שחפת סמויה, רעילות בכבד, לימפומה ואי ספיקת לב.
האתגרים שנותרו עם ביולוגים עבור פסוריאזיס כוללים: (1) להבין את המנגנון השולט בפסוריאזיס ודלקת מפרקים psoriatic; (2) להבין התגובות המטופל שונים לטיפול; (3) מנבא תגובה קלינית לפני או בתחילת הטיפול; (4) לפתח ניסוחים אוראלי, inhaled, ו אקטואלי; ו (5) לקבוע אם הטיפול משנה תוצאות longterm.
חומצה Fumaric היא טיפול פסוריאזיס העיקרי בגרמניה. זה מקטין ציטוקינים תלויי תא, אבל הוא לא יעיל כמו טיפולים קונבנציונליים אחרים, ונושאת סיכון גבוה של רעילות אי סבילות במערכת העיכול.
מתן טיפולים סיבוביים ומשולבים מגביר את היעילות ומפחית את הרעילות של הטיפול. העתיד עשוי להביא טיפול בתאי גזע וטיפולים מבוססי גנים, כולל טיפולי אנטי-סנס המעכבים ישירות גנים ספציפיים לפסוריאזיס. עם זאת, ההשפעות השליליות והרעילות של טיפולי פסוריאזיס קונבנציונליים מחייבות טיפולים טבעיים בטוחים ויעילים יותר שיכולים לשמש כחלופות או בצורה אינטגרטיבית.
טיפולים טבעיים עבור פסוריאזיס
דִיאֵטָה
גישה המבוססת על ראיות מציעה פסוריאזיס, המהווה למעשה הפרעה דלקתית, צריכה להפיק תועלת מתזונה אנטי-דלקתית, זיהוי, חיסול ו / או סיבוב של מזונות אלרגניים וצום טיפולי. 28-30 למרות שאין נתונים שפורסמו על הימנעות מאלרגיה למזון , חולי פסוריאזיס רבים מראים רגישות מוגברת לתסמיני הגלוטן והפסוריאזיס שלהם משתפרים בדיאטה נטולת גלוטן. 31 מדידת נוגדנים לטרנסגלוטמינאז וגליאדין של רקמות יכולה לסייע בזיהוי תת-קבוצה זו. הראיות גם מציע שמירה על משקל בריא יתרונות פסוריאזיס חולים, מאז פסוריאזיס חיובי בקורלציה עם מדד מסת הגוף גדל. 32
האיזון בין איקוסנואידים פרו-דלקתיים ואנטי-דלקתיים מושפע במידה רבה מסוג חומצות השומן התזונתיות הנצרכות. תזונה אנטי דלקתית מורכבת בעיקרה מדגש על "שומנים טובים" (דג מים קרים, אגוזים, זרעים, שמן זית, שמנים אחרים באיכות גבוהה), דגנים מלאים, קטניות, ירקות ופירות והימנעות מ"שומנים רעים" (רוויים). שומנים מהחי, שומני טראנס, מזון מטוגן ומעובד, שמנים באיכות ירודה) ופחמימות מזוקקות. בנוסף, כמות מוגזמת של חומצות שומן אומגה 6 בתזונה יכולה לתרום לתגובה דלקתית.33 המקורות העיקריים של שמני אומגה 6 בתזונה הם שמנים צמחיים כגון תירס, סויה, חריע וחמניות, בעוד המקורות העיקריים של חומצה ארכידונית הם בשר, ביצים ומוצרי חלב.
פרוסטגלנדין E2 (PGE2) הוא איקוסנואיד בולט המופק מחומצת השומן אומגה 6 ארכידונית. פעולה דומיננטית של PGE2 כמולקולת שליח היא לשפר את הרגישות בנוירוני כאב, להגביר את הנפיחות ולכווץ כלי דם. צריכת יתר של שמני אומגה 6 מספקת עודף מצע לסינתזה של PGE2, המניע תגובה דלקתית אגרסיבית ומתמשכת. פרוסטגלנדין E3 (PGE3) הוא�מופק מחומצת השומן אומגה 3, חומצה איקוספנטאנואית (EPA). רמות גבוהות יותר של PGE3 מפחיתות רגישות לכאב, מרפות כלי דם, מגבירות את זרימת הדם ותומכות בתגובה אנטי דלקתית טבעית של הגוף (איור 1).
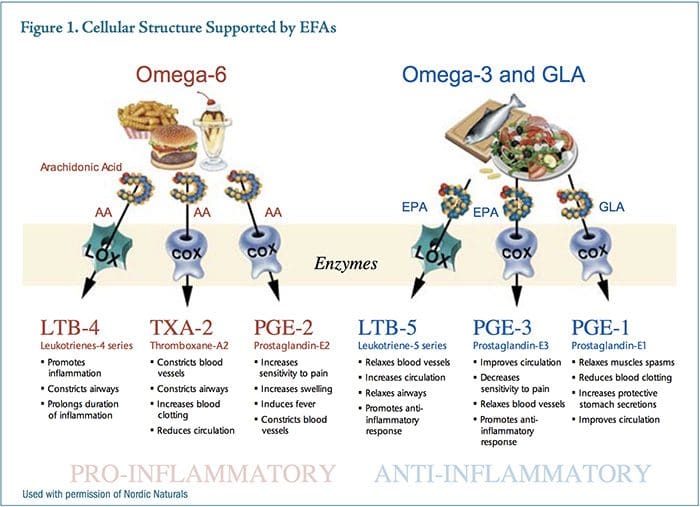
בעוד ששניהם PGE2 ו- PGE3 נחוצים להומיאוסטזיס תקין, הכמויות היחסיות של מולקולות השליחים המתחרות הללו תורמות או מקטינות תסמונות דלקתיות כרוניות. EPA הוא חשב לפעול על ידי מתחרים עם חומצה arachidonic עבור אתרי מחייב על cyclooxygenase-2 (COX-2), לייצר מתווך דלקתי פחות חזק, ולכן הפחתת דלקת. 34
לפני המהפכה התעשייתית, לא היו מקורות משמעותיים של אומגה 6 שמנים צמחיים בתזונה. רוב התרבויות צרכו דיאטות נמוכות בשמנים אלו וגבוהים בדגים או בבשר בקר או ביזון גבוה יותר באומגה- 3, ויצרו יחס של אומגה 6: אומגה 3 שהיה בערך 3: 1. המהפכה התעשייתית הביאה עימה את הידע והכלים לחידוש שמני הצומח, דבר שהביא לשינוי מהיר בהרגלי התזונה של רוב תרבויות המערב. יחס אומגה 6: אומגה 3 היה דחף במהירות לעבר האומדן הנוכחי של גבוה ככל 11: 1 אומגה 6: אומגה 3.35 גוף האדם לא היה מסוגל להסתגל גנטית לשינוי דרמטי זה צריכת חומצות שומן.
תרבויות מודרניות רבות צורכות כמויות גדולות של שמנים צמחיים, בעיקר במזונות מעובדים. לדוגמה, ייצור שמן סויה לצריכת מזון גדל פי 1,000 בין 1909 ו 1999.36 בנוסף, בעלי חיים, עופות ודגים מעובדים מוזנים תירס וקמח המבוסס על הזנה, אשר מעלה את התוכן אומגה 6 של בשר ודגים. כאשר בעלי חיים חקלאיים גדלים על דשא, תולעים או דיאטות טבעיות אחרות, הרקמות גבוהות יותר באופן טבעי בחומצות שומן אומגה-3. 37
תעשיית הבקר מציעה שיבוש במוצרי בקר מוגמרים, הודות למזון התירס והסויה. לבקר שניזון תירס וסויה יש תכולת חומצות שומן אומגה 6 גבוהה יותר בהשוואה לבקר שניזון בעשב. בעוד שבקר המוזן בעשב יכול להכיל עד 4 אחוז חומצות שומן אומגה 3, בקר שניזון תירס מכיל בדרך כלל 0.5 אחוז אומגה 3
התזונה האמריקאית הסטנדרטית מספקת יחס אומגה 6:אומגה 3 ממוצע של כ-11:1. תזונה המבוססת על צמחונים עלולה לסכן אדםאכילה של כמויות גדולות של שמנים צמחיים ומוצרי סויה, כמויות נמוכות של דגים, אשר יכול להטות את האיזון לכיוון פרו דלקתיים המדינה. צמצום שומנים צמחיים תזונתיים והגברת שומני אומגה-3 EPA וחומצה docosahexaenoic (DHA) על ידי צריכת דגים שומניים כמו בקלה, סלמון, מקרל וסרדינים יכולים להועיל לאנשים החווים מצבים דלקתיים כרוניים. 33
מספר עשבי תיבול המשמשים כתיבול, כולל כורכום, פלפל אדום, ציפורן, ג'ינג'ר, כמון, אניס, שומר, בזיליקום, רוזמרין, שום ורימון, יכולים לחסום את הפעלת הגורם הגרעיני-kappaB (NF?B) של ציטוקינים דלקתיים.38
גישות תזונתיים שמשפיעות על צריכת חומצות שומן יכולות להשפיע על הפרופיל האיקוסנואי בצורה כזו שתהליכים דלקתיים כגון ייצור חומצה אראצ'ידונית ותפעול תאי T מתחלפים, ואילו ציטוקינים כגון אינטרליוקין-4 (הציטוקין הראשוני האחראי לגירוי תגובה חיסונית של TH2 ) הם upregulated.34
תוספת תזונתיים
חומצות שומן חיוניות
חומצות שומן חיוניות (EFA) משפיעות על הפתופיזיולוגיה של פסוריאזיס בשלוש דרכים: ראשית, EFAs משפיעים על הקינטיקה של ממברנות התא; שנית, EFAs משפיעים על זרימת דם עורית ואפידרמיסית באמצעות תפקוד אנדותל משופר; ושלישית, EFAs פועלים כסוכן אימונומודולנטי דרך השפעתם על איקוסנואידים. EFAs משמשים כמצעים בסיסיים בפיתוח דו-שכבת הפוספוליפידים כמעט בכל תא בגוף האדם, כולל הדרמיס והאפידרמיס. הם יוצרים שלמות מבנית המווסתת את הנזילות, מה שמשפיע על הובלת תאים, קישור שליח ותקשורת תאים. חומצות שומן אומגה 3 יכולות לפעול הן במישרין והן בעקיפין על תפקוד האנדותל על ידי הפחתת ציטוקינים של תאים חד-גרעיניים כגון IL-1 ו-TNF?, 39 הפחתת היווצרות של גורם גדילה שמקורו בטסיות חלבון (PDGF), הגדלת הזמינות הביולוגית של תחמוצת החנקן. , והפחתת ביטוי של מולקולות הידבקות. ההשפעה המצטברת המווסתת את המתווכים הביו-אקטיביים הללו היא מניעת וסקולריזציה, או צמיחת כלי דם חדשים בתוך הרובד הפסוריאטי, ובו זמנית מאפשרת זלוף משופר של רקמת העור.
רכיבי החסינות הטבעית והרכישה, כולל הפקת מאפננים חיסוניים מרכזיים, עלולים להיות מושפעים מאומגה 3 ו- 6. ההשפעות החיסונית של חומצות שומן אומגה 3 כוללות דיכוי של lymphoproliferation, CD4 + תאים, מצגת אנטיגן, מצגת מולקולה הדבקה, תשובות TH1 ו Th2, ייצור ציטוקינים דלקתיים פרו. 34
כמה מחקרים הוכיחו את היתרונות של תוספת לווריד או דרך הפה של שמן דגים עבור פסוריאזיס. 40-42 במחקר שנערך על ידי Mayser et al, עירוי תוך ורידי של חומצות שומן אומגה 3 הוביל לעלייה בלוקוטרינים נוגדי דלקתיות B5 (LTB5) בתוך 4-7 ימים של תחילת הטיפול, בהשוואה לחולים שליטה. 43 בניסוי זה, חולים קיבלו אומגה 3 או אומגה 6 הכנה פעמיים ביום במשך 10 ימים. לא נצפו תופעות לוואי.
EPA מתחרה בחומצה אראצ'ידונית (AA) עבור 5-lipoxygenase ומייצרת LTB5, שהיא רק עשירית כמו עוצמה כמו המתווך הדלקתי leukotriene B4 (LTB4). רמות LTB4 הוכחו להיות גבוהות ב ploriques psoriatic ולהפגין תכונות chemotactic הדרושים חדירה של לויקוציטים וקרניוציטים התפשטות. 43
מאמר הסקירה של Ziboh על אומגה 3 ופסוריאזיס מתייחס לשישה מחקרים שנערכו באמצעות תוספי שמן דגים דרך הפה עם תוצאות מעורבות. למרבה הצער, לא ניתן למצוא הפניות מקוריות. שני מחקרים היו כפול-סמיות ומבוקר פלצבו, תוך שימוש ב-1.8 גרם EPA ו-DHA במהלך קורסים של שמונה שבועות ו-12 שבועות. המחקר בן שמונה השבועות הראה תועלת בגירוד, קנה המידה ואריתמה, בעוד שהמחקר בן 12 השבועות לא הראה שום תועלת.44
שלושה מחקרים פתוחים נערכו, מתן 10-18 G EPA ו- DHA מדי יום במשך שמונה שבועות. כל המחקרים הראו שיפור, כאשר שני מחקרים מדגימים מתון עד בינוני ומחקר אחד מדגים שיפור מתון עד מעולה בגלישה, גירוד ועובי הנגע. מחקר אחד בשילוב עם דיאטה דלת שומן הראה ירידה משמעותית בסימפטומים psoriatics.44,45
מספר מחקרים חקרו את השימוש בשמן דגים אקטואלי בריכוזי EPA משתנים. כמה מחקרים דיווחו על יתרונות, לרבות הפחתה בעובי הפלאק ובדרוג.46,47 במחקר אחד של Puglia וחב', תמציות שמן דגים וקטופרופן יושמו באופן מקומי על�נגעים psoriatic, עם ירידה נצפתה erythema.48 החיסרון המשמעותי ביותר ליישום שמן דגים מקומי הוא עמידה בשל הריח.
שמן דגים הוכיח גם הוא מועיל בתנאים אוטואימוניים משותפים כגון דלקת מפרקים שגרונית (RA). 49 בעוד תוספי שמן דגים לא נעשה שימוש בניסויים קליניים לטיפול בדלקת מפרקים psoriatic, זה עשוי להיות מועיל בטיפול במצב זה, אשר קווי דמיון רבים ל- RA, כולל מנגנון דלקתי נפוץ חסין חוסר תפקוד.
חומצה פולית
טיפול ב- Methotrexate גורם למחסור בחומצה פולית. כפי שהוזכר לעיל, בחולים שקיבלו MTX לפסוריאזיס, תוספת חומצה פולית הפחיתה את ההיארעות של הפאטו-טוקסיות ואי-סובלנות במערכת העיכול, אך עלולה לפגוע ביעילות של MTX.24 כאשר משלימים עם חומצה פולית או טפסים פעילים, חומצה פולית או 5-methyltetrahydrofolate, המינון המומלץ הוא 1-5 מ"ג / יום.
חלבון מי גבינה מבודד
XP-828L הוא תוסף תזונתי חדש עשוי תמצית חלבון נגזר מי גבינה, אשר הוכח לאחרונה להיות מועיל פסוריאזיס. 50,51 פרופיל ביולוגי של XP-828L סביר בשל נוכחותם של גורמי גדילה, immunoglobulins, ופעיל פפטידים שנמצאו תמצית מי גבינה ספציפית זו. מחקר במבחנה הראה כי ל- 828L יש השפעות מווסתות של החיסון, כולל עיכוב ייצור ציטוקינים מסוג TH1, כגון IFN-G ו- IL-2, אשר עשויים להפוך אותו ליעיל בטיפול בהפרעות הקשורות ל- T-Xperx, כגון פסוריאזיס. 1
מחקר פתוח נערך על 11 חולים מבוגרים עם פסוריאזיס פלאק כרוני ויציב בשני אחוזים או יותר משטח הגוף הכולל. משתתפי המחקר קיבלו 5 גרם פעמיים ביום של XP-828L במשך 56 ימים. הערכות באמצעות ציוני PASI ו-PGA) בוצעו ביום המיון הראשוני ושוב בימים 1, 28 ו-56. בסיום המחקר, לשבעה מתוך 11 הנבדקים היה ציון PASI מופחת שנעים מ-9.5 אחוזים ל-81.3 אחוזים.50 התוצאות של כפול סמיות גדול יותר,�מחקר מבוקר פלצבו בקרב 84 אנשים עם פסוריאזיס קלה עד בינונית הראה כי XP-828L (5 גרם ליום במשך 56 יום) הפחית משמעותית את ציון ה- PGA בהשוואה לפלצבו (p <0.05). לא נרשמו השפעות שליליות מצד משתתפי המחקר בשני המחקרים
ויטמין D
הוכח כי לחולים עם פסוריאזיס מפושטת יש ירידה משמעותית ברמות הסרום של הצורה הפעילה ביולוגית של ויטמין D, 1-alpha,25-dihydroxyvitamin D3 (1-?,25(OH)2D3; קלציטריול) בהשוואה לגיל ולמין. -התאימו לבקרות וגם בהשוואה לחולים עם פסוריאזיס בינוני.53 האם זה גורם תורם לפסוריאזיס או תוצאה של ההפרעה לא הובהר.
קרטינוציטים באפידרמיס הופכים 7-דהידדרוכולסטרול לויטמין D3 בנוכחות UVB. אור שמש, פוטותרפיה ב-UVB, קלציטריול דרך הפה, ואנלוגים מקומיים של ויטמין D הם טיפול יעיל בפסוריאזיס הודות לפעולות האנטי-התרבותיות והפרו-בידול של ויטמין D על קרטינוציטים.54-56
קלציטריול מחייב קולטני ויטמין D (VDR) בעור מאפנן את הביטוי של מספר רב של גנים, כולל הרגולטורים מחזור התא, גורמי גדילה, הקולטנים שלהם. פולימורפיזם של גן ה- VDR קשור לפסוריאזיס ועשוי להשפיע על התפתחות של פסוריאזיס והתנגדות לטיפול ב- calcipotriol, וכן לתרום לתפקוד הכבד בחולים עם פסוריאזיס. 57
בהתחשב בחשיבות של ויטמין D בפסוריאזיס, סרטן, מחלות דלקתיות ומצבים אחרים, הוצע על ידי כמה חוקרים שייתכן שיהיה צורך להעריך מחדש המלצות להגנה מפני השמש ומניעת סרטן העור כדי לאפשר מצב של ויטמין D מספיק. מחקר שנערך לאחרונה הראה שחשיפה מרובה לשמש במדגם של מבוגרים בהוואי לא בהכרח הבטיחה התאמה של ויטמין D, מה שמצביע על הצורך בתוסף ויטמין D כדי להשיג רמות אופטימליות בדם.58
מחקרים הוכיחו כי ויטמין D אוראלי ניתן לקחת בבטחה במינונים היומי של עד 5,000 IU, עם כמה מומחים ממליצים עד 10,000 IU היומי כדי לתקן חסר. 59-61 אוראלי ו אקטואלי ויטמין D, אור השמש, ו UVB phototherapy הראו יעילות רבה בטיפול בפסוריאזיס. 56
טיפולים אקטואלי של פסוריאזיס
מספר טיפולים מקומיים לפסוריאזיס עשויים לספק תועלת, כולל קלציפוטריאן (Dovonex�; אנלוגי ויטמין D3 סינתטי), קרם Berberis aquifolium (10%) 62 (פסוריפלורה�; Relieva�), ג'ל כורכומין (1%), אלוורה ו- משחה עשירה בפלבנואידים (Flavsalve�).
ג'ל כורכומין הניב רזולוציה של 90 אחוזים של פלאקים ב-50 אחוז מהחולים תוך 2-6 שבועות; שאר נבדקי המחקר הראו שיפור של 50 עד 85 אחוזים. נמצא כי כורכומין יעיל פי שניים מקרם קלציפוטריול (שלרוב לוקח שלושה חודשים להפעיל את מלוא השפעתו). המנגנון של כורכומין הוא מעכב פוספורילאז קינאז סלקטיבי, ובכך מפחית את הדלקת באמצעות עיכוב של NF?B.63
ניסוי מבוקר של קרם תמצית אלוורה (0.5%) בקרב 60 חולים במשך 4-12 חודשים הדגים ניקוי משמעותי של פלאקים פסוריאטיים (82.8%) בהשוואה לפלצבו (7.7%) (p <0.001). בנוסף, ה- PASI ירד לממוצע של 2.2.64
קשקשת הפסוריאזיס מועילה מהשימוש בחומרים מרככים. ליפידים בין-תאיים כגון סרמידים (מולקולות שומנים המורכבות מחומצות שומן וספינגוזין) ממלאים תפקיד חשוב בוויסות ההומאוסטזיס של מחסום העור-מים ויכולת החזקת המים. הוכח שסרמידים מופחתים באפידרמיס הפסוריאטי. חומרים מרככים חדשים יותר המכילים ceramide (למשל, CeraVe�, Mimyx�, Aveeno Eczema Care) הראו תועלת בפסוריאזיס ועשויים לשפר את תפקוד מחסום העור ולהפחית את איבוד המים.65
השפעות בוטניות
פורמולת צמחי מרפא סינית (Herose� Psoria Capsule) הוכיחה בטיחות ויעילות בטיפול בפסוריאזיס רובד חמור.66 Herose מורכב מקנה שורש Zingiberis, radix Salviae miltiorrhizae, radix Astragali, ramulus Cinnamomi, radix Paeoniae semopsis ו-pilenxos קויצ'יס. בניסוי פתוח, 15 נבדקים לקחו ארבע כמוסות Herose (450 מ"ג כל אחת) שלוש פעמים ביום במשך 10 חודשים. החוקר העריך את ה-PASI ואת התגובה הטיפולית להרוס עבור כל מטופל. הפורמולה מיועדת לחימום היאנג וקידום זרימת הדם.
התערבויות בסגנון חיים
גורמי סגנון חיים כגון עישון סיגריות וצריכת אלכוהול קשורים בחומרה של פסוריאזיס. 67 פעילות גופנית ופעילויות חוץ (נקיטת אמצעי זהירות לא כוויות שמש) מועילות. 68 רחצה ושיזוף בים המלח במשך ארבעה שבועות הביאה לירידה של PASI 81.5 אחוז, ירידה של 78 אחוז ב hyperplasia keratinocyte, כמעט חיסול מוחלט של לימפוציטים T מן האפידרמיס, עם מספר נמוך שנותר dermis.69
ניהול מתח יכול להועיל לאנשים עם פסוריאזיס. נבדקים שהאזינו לקלטת מדיטציה מודרכת בזמן שעברו פוטותרפיה, נמחקו פי ארבעה מהר יותר מאלה שקיבלו פוטותרפיה בלבד, כפי ששפטו שני רופאי עור עצמאיים. סטטוס הפסוריאזיס הוערך בשלוש דרכים: בדיקה ישירה על ידי אחיות המרפאה; בדיקה ישירה על ידי רופאים העיוורים למצב המחקר של המטופל (קלטת או ללא קלטת); והערכת רופא עיוור של צילומים של נגעי פסוריאזיס. ארבעה אינדיקטורים עוקבים של מצב העור נוטרו במהלך המחקר: נקודת תגובה ראשונה, נקודת מפנה, נקודת חצי ונקודת ניקוי. הנבדקים בקבוצות הקלטת הגיעו לנקודת המחצית (p=0.013) ולנקודת הסרה (p=0.033) מהר יותר באופן משמעותי מאלה במצב ללא קלטת, הן עבור טיפולי UVB והן עבור טיפולי PUVA.70 לבסוף, פסיכותרפיה יכולה להיות חיונית תוספת עבור אנשים עם בעיות פסיכולוגיות בלתי פתורות מתמשכות כמו חרדה, דיכאון ומתח פסיכו-סוציאלי של מחלת עור כרונית זו.
דיון
פסוריאזיס מאופיינת בהפעלה של תאי T המשחררת ציטוקינים פרו-דלקתיים כגון TNF-?, המובילים לשגשוג קרטינוציטים ולנגעי העור האופייניים לפסוריאזיס.
הגישה הקונבנציונלית לפסוריאזיס מורכבת משימוש בקורטיקוסטרואידים מקומיים ו/או דרך הפה, תרופות מדכאות חיסוניות אחרות, רטינואידים דרך הפה, אור UV, וכמה (לא בהכרח חדשניים, לאחר ששימשו בעבר למחלת קרוהן ו-RA) ביולוגיים. למרות שטיפולים אלו יכולים להיות יעילים מאוד בשליטה במחלה, אף אחד מהם אינו בטוח ויעיל באופן אוניברסלי, ולכל אחד מהם יש פרופיל סיכון ניכר.
ישנן עדויות לשימוש בשינוי תזונתי ובשמן דגים כדי להפחית את הדלקת בפסוריאזיס. יש צורך במחקר נוסף כדי להבהיר את השימוש�של אלה וטיפולים בוטניים מקומיים שונים והתערבויות אורח חיים לשיפור התסמינים הקליניים, הפחתת הביטוי פנוטיפי של פסוריאזיס, מתן טיפולים בטוחים ויעילים.